May 20 2022
/
Assorbimento d’acqua delle pelli e modello per la determinazione dell’acqua interagente – Parte II
L’articolo che leggerete è la seconda parte del contributo comparso sulla Leather Update #19/2022 ed è frutto della collaborazione tra il dottor Nogarole della SSIP e l’ingegner Pistorio.
Assorbimento d’acqua delle pelli e modello per la determinazione dell’acqua interagente – Parte II
Assorbimento d’acqua da parte del collagene
L’acqua associata alle proteine viene divisa in tre diverse categorie:
– acqua strutturale;
– acqua legata o vincolata;
– acqua libera.
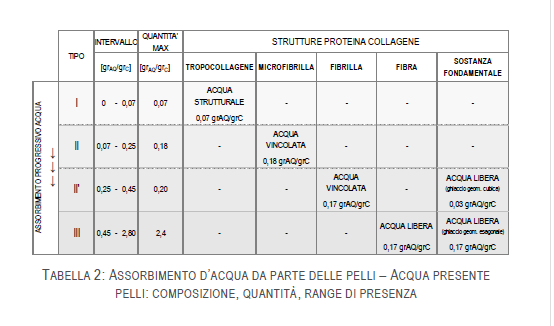
L’acqua strutturale è quella associata alla struttura della proteina e che può essere descritta da una stechiometria specifica (moliH2O/moliPR). In una scala ipotetica che parte da zero, l’acqua strutturale rappresenta la prima parte dell’acqua presente e, nel collagene, la sua quantità va da 0,00 a 0,07 gAQ/gCOLL. Quest’acqua è sempre presente nella proteina e la sua rimozione porta alla denaturazione del peptide perché, per farlo, se ne aggredisce la struttura.
L’acqua strutturale è quella che non è strutturale ma che presenta un legame con la proteina. Può essere definita come acqua legata alla proteina che presenta proprietà nettamente diverse da quelle dell’acqua libera, valutate con le stesse tecniche di misurazione1. La quantità dell’acqua legata è più alta di quella strutturale e, nel collagene, il suo valore è generalmente pari a 0,35 gAQ/gCOLL. Come vedremo, la presenza dell’acqua legata si estende all’interno dei Regimi II e II’. Un altro termine usato per definire l’acqua legata è quello di VINCOLATA, per indicare che la sua presenza non è libera ma è legata da vincoli di interazione con il peptide. Infine l’ACQUA LIBERA è quella che è presente nella proteina come acqua sfusa ed ha le funzioni di agente riempiente, facilmente rimovibile.
Esiste un quarto tipo di acqua che viene definita ACQUA DI TRANSIZIONE perché presenta proprietà che ricordano, in parte, quelle dell’acqua legata ed in parte quelle dell’acqua libera e che, nel presente lavoro, non interessano.
Nel collagene queste categorie si combinano tra loro all’interno di quelli che sono stati chiamati REGIMI o TIPI DI ACQUA e che sono quattro: Tipo I, Tipo II, Tipo II’ e Tipo III. Le definizioni di Tipi o Regimi sono state proposte nel 1977 da alcuni studiosi2 che hanno analizzato la presenza di acqua all’interno del collagene (tessuto dura madre HDM), definendo le proporzioni dei diversi tipi di acqua rispetto alla quantità della proteina e la loro distribuzione all’interno del tessuto cutaneo. Per fare questo, hanno analizzato le condizioni dell’acqua mediante diffrazione a raggi X su campioni di pelli ghiacciate. Il fatto che le pelli fossero ghiacciate ha permesso loro di osservare le geometrie dei cristalli di ghiaccio che si andavano formando (esagonale e cubica) consentendo ai ricercatori di ricavare ulteriori informazioni in merito alla presenza o meno di vincoli che legassero l’acqua alla proteina. Attraverso la spettroscopia meccanica dinamica, integrata da misurazioni della diffrazione dei raggi X a basse temperature, i ricercatori sono riusciti a capire quali fossero le interazioni esistenti tra acqua e collagene ed ha permesso loro di capire le relazioni che legano la struttura proteica e la risposta del tessuto collagenico alle sollecitazioni meccaniche, dato che quest’ultime dipendono dall’interazione della proteina con sostanze con cui è a contatto, ovvero con l’acqua. In merito all’acqua, l’effetto più rilevante dovrebbe essere atteso da quella frazione che interagisce con maggiore intensità con la proteina stessa: (strutturale→vincolata→libera).
Le misurazioni meccaniche dinamiche sono state effettuate utilizzando un pendolo torsionale invertito con oscillazione libera a circa 1 Hz nell’intervallo di temperatura 80°-280°K (-80°C-0°C). A causa della non uniformità nelle dimensioni dei provini, per il confronto dei risultati dei test di rigidità si è preferito usare la grandezza della RIGIDITÀ RELATIVA (Grel):

Sono stati evidenziati tre cambiamenti nel comportamento specifico del collagene che hanno permesso di identificare i diversi tipi di acqua ed i relativi contenuti di acqua specifici. Questi sono pari a 0,07, 0,25 e 0,45 gAQ/gC. Ancora, i test di diffrazione a raggi X hanno dimostrato l’esistenza di un po’ di acqua congelabile fino a contenuti d’acqua fino a 0,35 gAQ/gC, ovvero che, fino a contenuti d’acqua del 0,35 gAQ/gC (quindi contenuti attribuibili all’acqua di Tipo II’), la frazione di acqua congelabile è molto bassa. Come se non bastasse, la prima acqua congelabile non ha le stesse proprietà dell’acqua sfusa e congela formando cristalli a geometria cubica (meno comune) quando il raffreddamento è rapido.
Anche i test di rigidità hanno permesso di identificare tre differenti Tipi di acqua:
– sotto 0,25 gAQ/gC dove l’acqua ha un effetto irrigidente;
– tra 0,25 e 0,45 gAQ/gC, in cui l’acqua ammorbidisce la struttura del collagene;
– sopra 0,45 gAQ/gC, in cui è presente acqua congelabile che funge da riempitivo.
Nel loro studio, i ricercatori hanno dimostrato come i parametri meccanici dinamici (temperatura di picco, intensità, rigidità, ecc.) non variano uniformemente con il contenuto d’acqua ma descrivono alcune relazioni stechiometriche empiriche che legano il contenuto d’acqua alla struttura del collagene. Il collagene è organizzato in entità fibrose a vari livelli di organizzazione3:
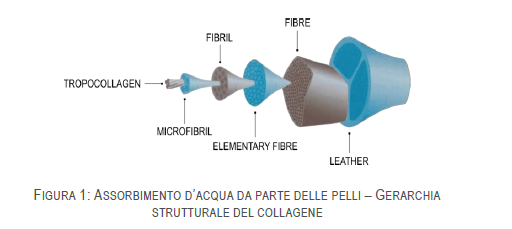
Le unità coinvolte nella gerarchia strutturale iniziano dai singoli amminoacidi che si associano in triple eliche di TROPOCOLLAGENE. Il tropocollagene è l’unità fondamentale del collagene e, in alcune pubblicazioni, viene indicato con il termine di MOLECOLA DI COLLAGENE. Cinque unità di tropocollagene formano un’entità fibrosa più grande a geometria pentagonale chiamata MICROFIBRILLA DI SMITH. Le microfibrille sono impacchettate in un reticolo tetragonale che si estende lateralmente per formare le FIBRILLE. Nel collagene in vita, queste iniziano ad essere circondate dalla sostanza fondamentale, che è una matrice esterna, un gel composto da acqua e mucopolisaccaridi. La struttura fibrille + sostanza
fondamentale si estende lateralmente per formare le FIBRE ELEMENTARI di collagene:

Gli elementi strutturali hanno andamento lineare e l’intreccio fibroso tipico delle fibre di collagene inizia a partire dalle fibre elementari. Queste si associano in FIBRE che, assieme a quelle reticolari ed elastiche, completano la formazione del tessuto collagenico.
Possiamo capire meglio come si dispone l’acqua all’interno del collagene immaginando un assorbimento progressivo d’acqua.
L’acqua più fortemente interagente con la proteina è quella del Tipo I, perché è quella che va a costituire il guscio d’acqua esterno alle triple eliche. La presenza del guscio d’acqua esterno è stata trattata nel 19954 ed i due gruppi di scienziati sono arrivati pressoché alle stesse conclusioni.
L’acqua più fortemente interagente con la proteina è quella del Tipo I, perché è quella che va a costituire il guscio d’acqua esterno alle triple eliche. La presenza del guscio d’acqua esterno è stata trattata nel 19954 ed i due gruppi di scienziati sono arrivati pressoché alle stesse conclusioni.
L’acqua di TIPO I è composta da acqua strutturale. La sua quantità massima è di 0,07 gAQ/gC ed è quella che è presente nell’intervallo di assorbimento iniziale (0-0,07 gAQ/gC). Non può essere scambiata e non partecipa a interazioni con nessun reagente perché è ciascuna molecola di acqua è legata al collagene per mezzo di due legami-H. Non congela, indice che le interazioni con il collagene sono molto forti. Quando viene rimossa dalla proteina, questa sì denatura senza possibilità di recupero perché le triple eliche collidono tra loro:
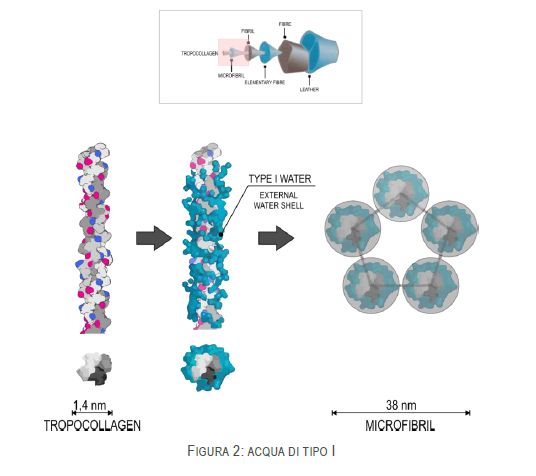
L’acqua del TIPO II si trova nelle regioni inter elicoidali, ovvero negli spazi tra triple eliche diverse, siano essi della stessa microfibrilla (cinque eliche di tropocollagene) o di microfibrille differenti. Si localizza in prossimità delle zone polari delle catene laterali formando sfere di idratazione che circondano i gruppi ionici di queste. L’interazione tra la proteina e l’acqua di Tipo II non è così forte come nel caso dell’acqua strutturale, ma quest’acqua influisce sulla rigidità in misura maggiore rispetto alla prima perché influenza le possibilità di scorrimento reciproco delle catene laterali:
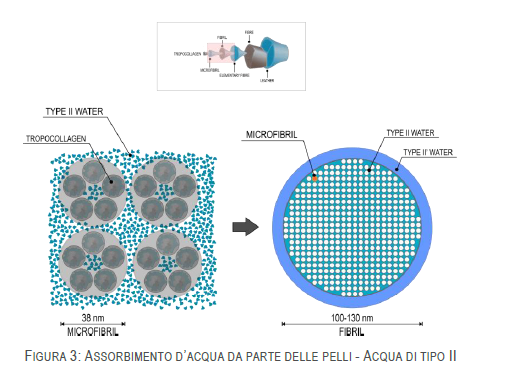
L’acqua di TIPO II’ ha caratteristiche intermedie tra quella di Tipo II e il III. Si tratta di acqua di transizione in cui una parte presenta alcune proprietà dell’acqua vincolata e in cui una parte presenta alcune proprietà dell’acqua libera (vedi dopo). Le differenze più marcate riguardano proprio l’acqua libera perché, quando il campione di pelle viene congelato, il ghiaccio che si forma presenta geometria cubica anziché la più comune esagonale. Qualunque sia la geometria dei cristalli, questi sono comunque troppo grandi per essere alloggiati all’interno delle fibrille e ciò significa che l’acqua libera del Tipo II’, come quella del Tipo III, è presente attorno alle fibrille e non in profondità maggiori. Per questo motivo è stato considerato che a profondità strutturali inferiori a quelle del livello fibrillare vi sia solo acqua di Tipo I e II. L’acqua vincolata continua a riempire le regioni intrafibrillari tra le molecole di tropocollagene e le microfibrille, ma è legata al collagene in maniera differente perché parte delle interazioni coinvolgono i legami peptidici. Rispetto all’acqua vincolata presente come acqua di Tipo II, quella presente come acqua di Tipo II’ presenta una maggiore capacità di interazione con i soluti.
L’acqua di Tipo II’ è costituita sia da acqua vincolata che da acqua libera e la sua quantità è pari a 0,20 gAQ/gC. È presente nell’intervallo di assorbimento da 0,25-0,45 gAQ/gC. La quantità dell’acqua vincolata può essere stimata come pari a 0,17 gAQ/gC mentre quella dell’acqua libera pari a 0,03 gAQ/gC e questo è il motivo per il quale il valore dell’acqua vincolata (totale) nel collagene arriva ad essere pari a 0,35 gAQ/gC. L’acqua di Tipo II’ presenta, mediamente, un punto di congelamento di -8,2 °C. Il legame con il collagene è quasi del tutto attribuibile all’acqua vincolata e si può dedurre che, in questa, le forze di legame siano assai inferiori rispetto a quelle dell’acqua vincolata che va a costituire l’acqua di Tipo II.
L’acqua di TIPO III è quella che, in condizioni fisiologiche, è presente all’interno della sostanza fondamentale. In condizioni non fisiologiche, è acqua che viene semplicemente assorbita dalle pelli e può arrivare ad essere pari a 2,7-2,8 gAQ/gC, ovvero pari a quasi tre volte la quantità di proteina:
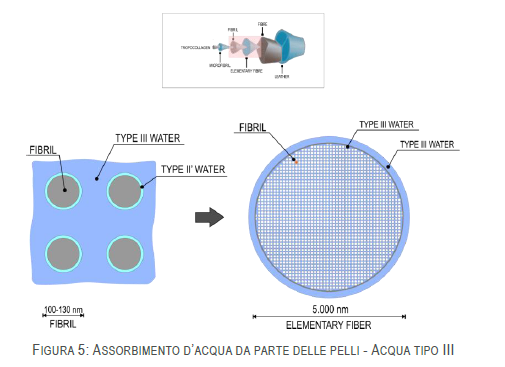
L’acqua di Tipo III è costituita interamente da acqua libera ed inizia ad essere presente quando l’assorbimento d’acqua diventa superiore a 0,45 gAQ/gC (considerando l’acqua libera nell’acqua di Tipo II’, l’assorbimento inizia a 0,42 gAQ/gC). Quando la pelle è immersa in acqua, l’acqua di Tipo III può arrivare ad essere pari a 2,3-2,5 gAQ/gC.
Come abbiamo visto, si tratta di acqua che non arriva fino all’interno delle fibrille, ma solo al loro esterno. Qualora riesca ad arrivare così in profondità, la sua caratterizzazione passa da acqua di tipo III ad acqua di tipo II. È molto probabile che continuino ad avvenire scambi di questo tipo.
A cura di Ing. Daniele Pistorio in collaborazione con
Marco Nogarole, Responsabile del Trasferimento Tecnologico della SSIP
Pubblicato il: 20 Mag 2022 alle 10:59

Related Posts

Pelli, il ruolo della Stazione Sperimentale per le imprese
Salatino: “Innovazione e sinergia”. Imperiale: “Riorganizzate le linee di ricerca” Il ruolo della Stazione Sperimentale…

Solofra, il distretto conciario riparte da depurazione e sostenibilità ambientale
Depurazione e sostenibilità ambientale. Parte da qui il progetto di rilancio del distretto conciario solofrano,…

Export: primato mondiale per la pelle italiana
Primato mondiale del Made in Italy: tra le prime 10 categorie di prodotto su 228,…

Lusso: il gruppo Louis Vuitton lancia La Maison des Startups per 50 talenti
Un nuovo programma di accelerazione dedicato alle start up. Questo è La Maison des Startups, il progetto…